Bonjour,
Voila je ne comprend la les expression de la théorie de Gillespsie, c'est a dire que je comprend pourquoi une molécule est AX1, AX2,AEX3,... mais je ne comprend pas pourquoi HCl est AX1 et que HBr est AE3X1.
Car le schéma de Lewis est le même pour le Br ou le Cl et le schéma ionique des deux molécules est identiques aussi. Alors je me demande pourquoi ils sont pas tous les deux la même expression selon la théorie de Gillepsie.
Je ne comprend pas non plus comment on sais si une molecule est polaire ou non. Dans mon cours on me dit qu'il faut trouver le centre de gravité mais on me dit que la molécule H2O est polaire et que H2S ne l'est pas alors qu'ils ont la même représentation sauf qu'ils ont une autre liaison convalente. Qqun sait m'expliquer?
Merci d'avance.
Geométrie des molecules(ions) + molecules polaire et non polaire
7 messages
- Page 1 sur 1
Gillespie
Il est clair que HCl, HBr et HI ont la même disposition, à savoir AX1E3. Mais il arrive que l'on oublie de mentionner les électrons E1 E2 ou E3.
De même H2O ou H2S sont décrits par : AX2E2.
H2O et H2S sont tous deux polaires. Mais H2S est beaucoup moins polaire que H2O.
Pour déterminer le moment dipolaire, tu dessines la molécule, puis tu remplaces les traits des liaisons de covalence par des vecteurs partant de l'atome central. La longueur de ces vecteurs est proportionnelle à la différence d'électronégativité. Pour H2O les vecteurs sont longs, car H et O ont des électronégativités très doifférentes : 2.2 et 3.5. Pour H2S ils sont presque 3 fois plus courts, car H et S ont des électronégativités voisines (2.2, et 2.7)
Tu détermines la résultante de ces deux vecteurs, avec la règle du parallélogramme. Plus la résultante est longue, plus la molécule est polaire. On voit que H2O est 2 à 3 fois plus polaire que H2S.
De même H2O ou H2S sont décrits par : AX2E2.
H2O et H2S sont tous deux polaires. Mais H2S est beaucoup moins polaire que H2O.
Pour déterminer le moment dipolaire, tu dessines la molécule, puis tu remplaces les traits des liaisons de covalence par des vecteurs partant de l'atome central. La longueur de ces vecteurs est proportionnelle à la différence d'électronégativité. Pour H2O les vecteurs sont longs, car H et O ont des électronégativités très doifférentes : 2.2 et 3.5. Pour H2S ils sont presque 3 fois plus courts, car H et S ont des électronégativités voisines (2.2, et 2.7)
Tu détermines la résultante de ces deux vecteurs, avec la règle du parallélogramme. Plus la résultante est longue, plus la molécule est polaire. On voit que H2O est 2 à 3 fois plus polaire que H2S.
Bon ben maurice a (très) bien répondu à ta deuxieme question. je vais donc me contenter de répondre à la premiere :happy2:
Alors déjà reprenons la base.
Une molecule est notée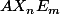 avec
avec 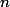 le nombre de liaisons que l'atome central (s'il existe, mais ca sera souvent le cas) fait avec les autres atomes qui l'entourent, et
le nombre de liaisons que l'atome central (s'il existe, mais ca sera souvent le cas) fait avec les autres atomes qui l'entourent, et 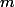 le nombre de doublets non liants présents ( donc jamais au delà de 3, tu t'en doutes...).
le nombre de doublets non liants présents ( donc jamais au delà de 3, tu t'en doutes...).
Un premier conseil: Attention à ne pas inverser le E et le X en notant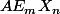 , c'est vraiment source de confusion. Garde toujours l'ordre
, c'est vraiment source de confusion. Garde toujours l'ordre 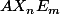 :happy2: .
:happy2: .
Je t'explique désormais ma technique, qui te permettra de trouver de façon infaillible la geometrie notée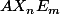 , du moins lorsqu'il éxiste un atome central.
, du moins lorsqu'il éxiste un atome central.
Premierement, toute cette technique repose sur la connaissance du nombre d'electrons situés sur la couche externe des atomes que tu vas étudier. Deux façon d'en trouver le nombre:
1/ La plus simple: tu prends un tableau de Mendeleïev
=> la derniere colonne, celle des gaz rares, est evidemment très stable donc possède 8 electrons sur sa couche externe. En reculant vers la colonne de B, tu perds un electron à chaque fois. Donc tu auras B ( 3 electrons couches ext), C (4), N( 5) etc etc...A ne pas confondre evidemment avec le numero atomique^^. La colonne de l'hydrogene en a 1 et celle du Beryllium 2. il me semble que ctete technique ne s'applique pas aux elements du centre du tableau. Mais bon, sachant que toute la colonne est concerné (c'est à dire que tous les elements de la colonne du carbone ont 4 electrons sur leur couche externe etc) tu as quand même en main une grande partie des infos utiles pour les éléments souvent utilisés.
2/ La plus longue mais qui marche pour tous: Il s'agit d'utiliser l'ecriture 1s^2, 2s^2, 2p^6 etc, mais cela suppose de la connaitre, et de bien savoir placer la barre séparant les electrons de coeur des electrons externes.
Mais revenons à nos moutons.
Donc:
Premiere etape: Trouver pour chaque atome de la molécule le nombre d'electrons externes.
Prenons l'exemple de la molécule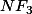
N, comme expliqué précédemment possède 5 electrons ext.
F, lui, en possède 7 (colonne du fluor).
En tout on a donc (3x7+5=) 26 electrons externes pour la molécule.
Voila ma technique: On divise ce nombre par 8. On obtient un premier nombre, le quotient, ici de 3, et un autre, le reste ici de 2. (8x3+2=26 je t'apprends rien lool).
Le premier chiffre, ici 3, correspond à ton n. C'est le nombre de liaisons fait par l'atome central avec les autres atomes.
Le deuxieme chiffre, ici 2, est le nombre d'electrons libre. Pour savoir le nombre de doublets non liants, on divise ce nombre par 2, puisqu'un doublet= deux eletcrons. On obtient le nombre de doublets non liants de l'atome central, c'est à dire m.
Ici, ca nous fera donc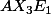 , ce qui correspond à l'image:
, ce qui correspond à l'image: 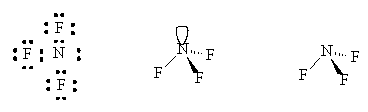
La sorte de bulle correspondant au doublet.
Avec cette technique, tu pourras normalment résoudre tous les problemes se posant avec un atome central, qui "lient" tous les autres.
Attention néanmoins

 Il existe une exception à la regle:!: L'hydrogene (H) ne doit pas etre compter avec 1 electron sur sa couche externe mais 7. [utile, parcque beaucoup de molécules ont des H ^^, et sinon ca foire]
Il existe une exception à la regle:!: L'hydrogene (H) ne doit pas etre compter avec 1 electron sur sa couche externe mais 7. [utile, parcque beaucoup de molécules ont des H ^^, et sinon ca foire]
Autre petite note: Pour les molécules ioniques, commence par calculer comme je l'ai fait sans prendre en compte
les ions. Puis rajoute ( si la molecule est negative) ou enleve (si elle est positive) au nombre totale, le nombre de charges.
Pour tes exemples, comme tu le vois il n'y a pas d'atome central. On résonne donc sur le nombre d'electrons externes.
Pour HCl. On note ca: H--Cl. Cl a (de lui meme) 7 electrons sur sa couche externe, ce qui signifie 3 doublets (non liants puisque couche externe+ un electron tout seul, utiliser pour faire la liaison avec le H). Si tu recomptes, tu en as bien 7 autour. HCl est donc non pas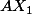 mais
mais 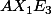 , si on prends comme "atome central" le Cl. Le probleme c'est que la il n'y en a pas reelement, c'est peut-etre pour ça qu'on oublie comme dit maurice le E3.http://www.elmhurst.edu/~chm/onlcourse/chm110/outlines/images/HCl.GIF
, si on prends comme "atome central" le Cl. Le probleme c'est que la il n'y en a pas reelement, c'est peut-etre pour ça qu'on oublie comme dit maurice le E3.http://www.elmhurst.edu/~chm/onlcourse/chm110/outlines/images/HCl.GIF
Avec le raisonnement que je viens de faire, je pense que tu as compris que HBr, lui aussi, est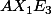 , toujours si on considere le Br comme "atome central".
, toujours si on considere le Br comme "atome central".
Voila, j'espere que ca t'aidera. peut-etre avais tu déjà tout compris, dans ce cas ca te fera une verif
UN ptit merci ne serait pas de refus :marteau:
@pluch!
Alors déjà reprenons la base.
Une molecule est notée
Un premier conseil: Attention à ne pas inverser le E et le X en notant
Je t'explique désormais ma technique, qui te permettra de trouver de façon infaillible la geometrie notée
Premierement, toute cette technique repose sur la connaissance du nombre d'electrons situés sur la couche externe des atomes que tu vas étudier. Deux façon d'en trouver le nombre:
1/ La plus simple: tu prends un tableau de Mendeleïev
=> la derniere colonne, celle des gaz rares, est evidemment très stable donc possède 8 electrons sur sa couche externe. En reculant vers la colonne de B, tu perds un electron à chaque fois. Donc tu auras B ( 3 electrons couches ext), C (4), N( 5) etc etc...A ne pas confondre evidemment avec le numero atomique^^. La colonne de l'hydrogene en a 1 et celle du Beryllium 2. il me semble que ctete technique ne s'applique pas aux elements du centre du tableau. Mais bon, sachant que toute la colonne est concerné (c'est à dire que tous les elements de la colonne du carbone ont 4 electrons sur leur couche externe etc) tu as quand même en main une grande partie des infos utiles pour les éléments souvent utilisés.
2/ La plus longue mais qui marche pour tous: Il s'agit d'utiliser l'ecriture 1s^2, 2s^2, 2p^6 etc, mais cela suppose de la connaitre, et de bien savoir placer la barre séparant les electrons de coeur des electrons externes.
Mais revenons à nos moutons.
Donc:
Premiere etape: Trouver pour chaque atome de la molécule le nombre d'electrons externes.
Prenons l'exemple de la molécule
N, comme expliqué précédemment possède 5 electrons ext.
F, lui, en possède 7 (colonne du fluor).
En tout on a donc (3x7+5=) 26 electrons externes pour la molécule.
Voila ma technique: On divise ce nombre par 8. On obtient un premier nombre, le quotient, ici de 3, et un autre, le reste ici de 2. (8x3+2=26 je t'apprends rien lool).
Le premier chiffre, ici 3, correspond à ton n. C'est le nombre de liaisons fait par l'atome central avec les autres atomes.
Le deuxieme chiffre, ici 2, est le nombre d'electrons libre. Pour savoir le nombre de doublets non liants, on divise ce nombre par 2, puisqu'un doublet= deux eletcrons. On obtient le nombre de doublets non liants de l'atome central, c'est à dire m.
Ici, ca nous fera donc

La sorte de bulle correspondant au doublet.
Avec cette technique, tu pourras normalment résoudre tous les problemes se posant avec un atome central, qui "lient" tous les autres.
Attention néanmoins
Autre petite note: Pour les molécules ioniques, commence par calculer comme je l'ai fait sans prendre en compte
les ions. Puis rajoute ( si la molecule est negative) ou enleve (si elle est positive) au nombre totale, le nombre de charges.
Pour tes exemples, comme tu le vois il n'y a pas d'atome central. On résonne donc sur le nombre d'electrons externes.
Pour HCl. On note ca: H--Cl. Cl a (de lui meme) 7 electrons sur sa couche externe, ce qui signifie 3 doublets (non liants puisque couche externe+ un electron tout seul, utiliser pour faire la liaison avec le H). Si tu recomptes, tu en as bien 7 autour. HCl est donc non pas
Avec le raisonnement que je viens de faire, je pense que tu as compris que HBr, lui aussi, est
Voila, j'espere que ca t'aidera. peut-etre avais tu déjà tout compris, dans ce cas ca te fera une verif
UN ptit merci ne serait pas de refus :marteau:
@pluch!
7 messages
- Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 3 invités
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
