3771 résultats trouvés
Revenir à la recherche avancée
Que faut -t-il retenir principalement de ce deuxième principe de thermodynamique ? :happy3: que dans une transformation reversible : $ dS = \frac{dQ}{T} $ ! c'est tout ? :happy3: Dans toute transformation, dS = dQ/T . Et dans tous les cas, \Delta S = \Delta Q/\Delta T . En gros, le 2e principe est ...
- 20 Mar 2010, 20:03
- Forum: ⚛ Physique
- Sujet: Entropie
- Réponses: 25
- Vues: 2245
Vous trouvez pas qu'il y'a un petit paradoxe dans ce texte : Parceque , d'un coté, il est dit que, l'entropie est maximale à l'équilibre thermodynamique, c'est à dire il ne peut aller plus que cette valeur maximale ( il peut pas aumenter ) . Par contre il est dit aussi que l'entropie augmente au co...
- 20 Mar 2010, 19:18
- Forum: ⚛ Physique
- Sujet: Entropie
- Réponses: 25
- Vues: 2245
Je répondrais bien "potentiel chimique constant", mais ca menera a un sujet "Potentiel chimique".
Donc...
http://fr.wikipedia.org/wiki/%C3%89quilibre_chimique
Donc...
http://fr.wikipedia.org/wiki/%C3%89quilibre_chimique
- 20 Mar 2010, 18:49
- Forum: ☣ Chimie
- Sujet: Equilibre chimique
- Réponses: 3
- Vues: 1544
barbu23 a écrit:c'est quoi un équilibre thermodynamique ? :hein:
Tu poses une question sans meme te préoccuper des définitions présentes dans cet énoncé?
Equilibre thermodynamique = Equilibre thermal (dT = 0) + Equilibre mecanique (dE = 0) + equilibre chimique (eta = 0).
- 20 Mar 2010, 18:10
- Forum: ⚛ Physique
- Sujet: Entropie
- Réponses: 25
- Vues: 2245
\gamma = \fr{c_p}{c_v} . Je n'ai qu'un seul exemple "récent": une molécule quelconque de l'atmosphere terrestre a \gamma = \fr{7}{5} , soit 3 degrés de liberté. Oui, mais si \gamma était inférieur à 1, le gaz refroidirait lors d'une compression j'ai l'impression. A+ Math Exact, et c'est i...
- 20 Mar 2010, 18:02
- Forum: ⚛ Physique
- Sujet: Compression et PV = nRT
- Réponses: 13
- Vues: 2982
? Tu as un procédé adiabatique. Par conséquent, dEint = nCvdT = - PdV car Eint f - E int i = Q + W avec Q = 0. En derivant correctemen PV = nRT on a Pdv + VdP = nRdT en utilisant la premiere equation, on substitue dT et on trouve PdV + VdP = - [R/Cv]*PdV Comme R = Cp - Cv, on obtient en divisant pa...
- 20 Mar 2010, 17:59
- Forum: ⚛ Physique
- Sujet: Compression et PV = nRT
- Réponses: 13
- Vues: 2982
Ah... Je ne connaissais pas ceci, Merci. J'imagine que dériver pV = nRT fera l'affaire pour la démonstration. Mouais. Bonne chance, dériver de facon théorique PV=nRT n'est pas simple; cette loi est, les 3/4 du temps, considérée comme un axiome, vu la difficulté (et le caractere circulaire lors de c...
- 20 Mar 2010, 17:54
- Forum: ⚛ Physique
- Sujet: Compression et PV = nRT
- Réponses: 13
- Vues: 2982
Ton changement est adiabatique. Donc, 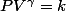 avec k,gamma constant, tout simplement
avec k,gamma constant, tout simplement 
Tu peux prouver tres facilement la relation en question.
Tu peux prouver tres facilement la relation en question.
- 20 Mar 2010, 17:43
- Forum: ⚛ Physique
- Sujet: Compression et PV = nRT
- Réponses: 13
- Vues: 2982
Bonjour, :happy3: Je cherche un exemple simple qui met en application, ce qui se dit dans le texte suivant : Pourquoi, lentropie est maximale à léquilibre thermodynamique ? Merci d'avance ! :happy3: Un équilibre thermodynamique est irréversible (i.e. il est impossible de "briser" l'équi...
- 20 Mar 2010, 17:34
- Forum: ⚛ Physique
- Sujet: Entropie
- Réponses: 25
- Vues: 2245
Bonjour, Demain, 14 mars, c'est le jour où l'on célèbre \pi aussi appelé le \pi -day Pourquoi 14 mars, car 14/03 (03-14 pour les anglais) Je voulais juste avoir votre avis sur ça, qu'en dites vous qu'a San fransisco Exploratorium, on défile dans les rues en récitant les décimales, et mange des tart...
- 14 Mar 2010, 15:37
- Forum: ⚜ Salon Mathématique
- Sujet: Célébration de Pi
- Réponses: 11
- Vues: 1168
lusky16 a écrit:donc5x4 ???
Tu as donc
- 14 Mar 2010, 15:23
- Forum: ✎ Collège et Primaire
- Sujet: Help DM pour le 15/03/10 compliqué
- Réponses: 16
- Vues: 1167
Bonjour, Est-ce que quelqu'un pourrait m'aider pour un exercice de maths assez difficile? Voici l'exercice sur les probabilités: On considère une particule ne pouvant occuper que deux positions A et B. Elle se déplace aléatoirement de l'une à l'autre de la façon suivante: Au temps 0, la particule e...
- 14 Mar 2010, 15:19
- Forum: ✎✎ Lycée
- Sujet: Urgentissime probabilités
- Réponses: 2
- Vues: 2767
- 14 Mar 2010, 15:08
- Forum: ✎ Collège et Primaire
- Sujet: Help DM pour le 15/03/10 compliqué
- Réponses: 16
- Vues: 1167
lusky16 a écrit:tu peux vraiment pas me donner la réponse s'il te plait car je ne comprend vraiment rien même avec des explications détaillés comme tu me le montre =(
k est un entier positif mais lequel et comment le trouver, je ne comprend pas
20 = 4 fois 5, non?
- 14 Mar 2010, 15:03
- Forum: ✎ Collège et Primaire
- Sujet: Help DM pour le 15/03/10 compliqué
- Réponses: 16
- Vues: 1167
je ne vois pas le rapport avec l'énoncé et l'émoticone mais bon, pas grave .... :hein: pour répondre à anima j'ai essayé de faire comme ceci : A= ;)5+20 A= V25 A= 5 mais je sais très bien que c'est n'importe quoi et que ce n'est pas la bonne réponse .... C'est effectivement completement faux. Si le...
- 14 Mar 2010, 14:14
- Forum: ✎ Collège et Primaire
- Sujet: Help DM pour le 15/03/10 compliqué
- Réponses: 16
- Vues: 1167
Probleme réglé. La page d'accueil est désormais mise a jour toutes les minutes, indépendamment des ajouts/suppressions de messages.
Merci d'avoir signalé ce petit bug. :++:
Merci d'avoir signalé ce petit bug. :++:
- 14 Mar 2010, 14:05
- Forum: ⚑ À propos de ce site
- Sujet: Faille dans le site ?
- Réponses: 5
- Vues: 2129
- 14 Mar 2010, 14:03
- Forum: ✎✎ Lycée
- Sujet: Dm de spécialité maths sur intégrale & dérivée
- Réponses: 10
- Vues: 1101
- 14 Mar 2010, 13:51
- Forum: ✎✎ Lycée
- Sujet: Dm de spécialité maths sur intégrale & dérivée
- Réponses: 10
- Vues: 1101
lol Oui je veut bien mais justement le but de pas le développé c'est de voir qu'on retrouve le même résultat entre f(x) et g(x) ! :+++: Je ne sais pas si ton énoncé cherche a te montrer que f(x)=g(x) ou si \int x^2 dx - \int x(x-1) dx = \int x dx . Tu peux tenter la 2e appro...
- 14 Mar 2010, 13:40
- Forum: ✎✎ Lycée
- Sujet: Intégrales !
- Réponses: 13
- Vues: 1077
Si tu me donnes une preuve irréfutable que tu as au moins essayé de faire ton DM, et si tu peux poster ton raisonnement et tes débuts de réponses, je suis sur que quelqu'un pourra t'aider. Le but du forum n'est pas de faire des DMs, mais d'aider les utilisateurs. Si notre seul role était d'écrire de...
- 14 Mar 2010, 13:35
- Forum: ✎ Collège et Primaire
- Sujet: DM pour demain 4 eme
- Réponses: 60
- Vues: 3172
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
