Bonjour a tous !Je suis sur mon DM de Chimie et j'ai un peu de mal sur certaine questions :
1. On fabrique de façon industrielle l'éthanol par addition d'eau sur l'éthène. Ecrire l'équation bilan de cette réaction chimique.
2.Lors de la combustion incomplète du propane C3H8 avec du dioxygène, il y a formation de carbone, de dioxyde de carbone et de vapeur d'eau.
Sachant que 3 moles de propane donnent 5 moles de carbone, écrire et equilibrer cette réaction.
Voilà en espérant que vous pourrez me venir en aide Bonne journée à tous !
Chimie organique
11 messages
- Page 1 sur 1
chimie organique
Et bien je bloque sur ces deux questions.
A vrai dire j'ai du mal a comprendre les réaction d'addition etc... et malgré mes cours ces deux questions me posent problème.
A vrai dire j'ai du mal a comprendre les réaction d'addition etc... et malgré mes cours ces deux questions me posent problème.
Ah oui au temps pour moi j'ai inversé les produits et les réactifs !
Et pour ma deuxième question je ne suis pas sure de moi en voulant écrire :
C3H8 + O2 (flèche) 3C + 3C02 + vapeur d'eau (étant donner que c'est une combustion incomplète). Mais on me dit " sachant que 3 moles de propane donnent 5 moles de carbone", sa me perturbe un peu car faut-il que se soit mes résultat lorsque j'équilibre mon équation?
Et pour ma deuxième question je ne suis pas sure de moi en voulant écrire :
C3H8 + O2 (flèche) 3C + 3C02 + vapeur d'eau (étant donner que c'est une combustion incomplète). Mais on me dit " sachant que 3 moles de propane donnent 5 moles de carbone", sa me perturbe un peu car faut-il que se soit mes résultat lorsque j'équilibre mon équation?
Pour ta 2ème question, il faut écrire une équation qui satisfasse aux exigences, à savoir que 3 moles de propane entrent en réaction, et qu'il se forme 5 moles de carbone. Cela veut dire que ton équation doit s'écrire :

Puisque tu introduis 9 atomes C dans tes 3 molécules , et que tu en récoltes cinq sous forme de C, il en reste 4 sous forme de
, et que tu en récoltes cinq sous forme de C, il en reste 4 sous forme de 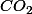 . Continue ! Equilibre la fin de cette équation ! On t'aidera si tu n'y arrives pas !
. Continue ! Equilibre la fin de cette équation ! On t'aidera si tu n'y arrives pas !
Puisque tu introduis 9 atomes C dans tes 3 molécules
Bon. Allons-y pas à pas.
J'espère que tu as compris que 3 fois et de l'oxygène forme 5 C et autre chose.
et de l'oxygène forme 5 C et autre chose.
Quand tu engages ces 3 molécules de propane , tu dois retrouver les 3·3 = 9 atomes C et les 3·8 = 24 atomes H qu'elles contiennent, sur le côté droite de l'équation.
, tu dois retrouver les 3·3 = 9 atomes C et les 3·8 = 24 atomes H qu'elles contiennent, sur le côté droite de l'équation.
Occupons-nous d'abord des atomes C du propane. Sur ces 9 atomes C, 5 se retrouvent sous forme C non combiné, à droite. Le restant, donc 9-5 = 4 atomes C se retrouvent sous forme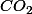 : on devra donc mentionner à droite de la flèche : 4
: on devra donc mentionner à droite de la flèche : 4 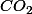 (pour autant qu'il y ait assez d'atomes O, mais de cela on s'en occupera plus tard.)
(pour autant qu'il y ait assez d'atomes O, mais de cela on s'en occupera plus tard.)
Occupons-nous maintenant des 24 atomes H du propane. Ils se retrouvent tous sous forme de molécules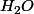 . Avec ces 24 H, qui se retrouvent groupés deux par deux, on peut faire 12 molécules
. Avec ces 24 H, qui se retrouvent groupés deux par deux, on peut faire 12 molécules 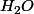 .
.
Avec cela, on a liquidé le problème des atomes des 3 molécules . Tu m'a suivi ?
. Tu m'a suivi ?
Reste à s'occuper des atomes d'oxygène. A gauche on ne sait pas encore combien il faudra en mettre. Par contre à droite on le sait. Mais c'est compliqué, car on en trouve dans les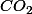 et dans les
et dans les 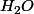 . Combien y en a-t-il en tout à droite ? Il y en a 4·2 = 8 dans les 4 molécules
. Combien y en a-t-il en tout à droite ? Il y en a 4·2 = 8 dans les 4 molécules 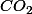 et 12 dans les 12 molécules
et 12 dans les 12 molécules 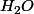 . Au total, 8 + 12 = 20 atomes O sont engagés à droite. On doit en retrouver le même nombre à gauche, donc 10, mais sous forme de molécules
. Au total, 8 + 12 = 20 atomes O sont engagés à droite. On doit en retrouver le même nombre à gauche, donc 10, mais sous forme de molécules 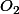 . Cela fait 10 molécules
. Cela fait 10 molécules 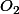 .
.
On est au bout de nos peines.
L'équation devient :
3 + 10
+ 10 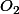 --> 5 C + 4
--> 5 C + 4 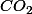 + 12
+ 12 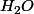
Tu m'as suivoi ?
J'espère que tu as compris que 3 fois
Quand tu engages ces 3 molécules de propane
Occupons-nous d'abord des atomes C du propane. Sur ces 9 atomes C, 5 se retrouvent sous forme C non combiné, à droite. Le restant, donc 9-5 = 4 atomes C se retrouvent sous forme
Occupons-nous maintenant des 24 atomes H du propane. Ils se retrouvent tous sous forme de molécules
Avec cela, on a liquidé le problème des atomes des 3 molécules
Reste à s'occuper des atomes d'oxygène. A gauche on ne sait pas encore combien il faudra en mettre. Par contre à droite on le sait. Mais c'est compliqué, car on en trouve dans les
On est au bout de nos peines.
L'équation devient :
3
Tu m'as suivoi ?
11 messages
- Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 3 invités
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
