Variation d'entropie
De la mécanique au nucléaire, nos physiciens sont à l'écoute
-
Tqup3
- Membre Naturel
- Messages: 74
- Enregistré le: 27 Mai 2006, 20:22
-
 par Tqup3 » 04 Juin 2006, 15:01
par Tqup3 » 04 Juin 2006, 15:01
Bonjour,
Voilà j'ai un petit problème...je n'arrive pas à retrouver la variation d'entropie pour une tranformation adiabatique irréversible...J'ai cherché partout et je trouve pas la réponse. dS vaut-il 0 ? Je ne crois pas puisque de l'entropie est créee normalement (Sc>0).
Ensuite, normalement pour une transformation irréversible, on calcule le Se (qui vaut 0 ici) et puis ensuite on calcule
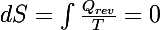
pour une transformation réversible puis on en déduit Sc mais dans le cas d'une transformation adiab et irréversible, on trouve 0.
Quelqu'un peut-il m'aider ??
Merci d'avance
-
cesar
- Membre Rationnel
- Messages: 841
- Enregistré le: 05 Juin 2005, 07:12
-
 par cesar » 05 Juin 2006, 08:48
par cesar » 05 Juin 2006, 08:48
bonjour,
peut on avoir le detail de votre probleme ??
par ailleurs : la formule dS = dQ/T n'est pas la bonne, c'est deltaQ/T. Le delta Q n'est pas une differentielle, sauf cas particulier. Donc votre integrale que vous donnez est fausse - ce que vous saviez dejà... car elle ne s'applique qu'au cas reversible....
-
Tqup3
- Membre Naturel
- Messages: 74
- Enregistré le: 27 Mai 2006, 20:22
-
 par Tqup3 » 05 Juin 2006, 10:53
par Tqup3 » 05 Juin 2006, 10:53
Voici mon exo, Je suis bloqué donc au calcul de l'entropie dans le cas de l'irréversibilité c'est à dire dans le II c) (ne pas préter attention aux réponses fausses du II a) (240K) et b) (-7000 J) à peu près je crois :

Est-ce que la formule :
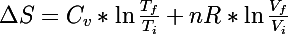
est utilisable dans les transformations irréversibles ???
Merci de votre aide.
-
cesar
- Membre Rationnel
- Messages: 841
- Enregistré le: 05 Juin 2005, 07:12
-
 par cesar » 05 Juin 2006, 15:36
par cesar » 05 Juin 2006, 15:36
la solution est dans le calcul du travail de transformation : il se fait en considerant que la pression exterieure est constante égale à P0. Cela donne l'état final. le gaz passe de la pression initiale à P0, ce qui permet de calculer les paramétres (T et P) de l'état final en passant par l'energie interne U.
c'est la question qui precede celle de l'entropie.
pour celle de l'entropie :
on a : delta Q = Cp*dT - v*dp
soit dS = Cp*dT/T - V*dp/T avec Cp=5/2*R*n, pour n moles de gaz ici n=1.
soit S = R*(5/2*ln(T) - ln(p)) + S0, S0 constante d'intégration.
d'où le calcul de la variation de S
delta S = R*(5/2*ln(T1/T0) - ln(p1/p0))
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 10 invités

