Une autre devinette de physique
De la mécanique au nucléaire, nos physiciens sont à l'écoute
 par Dominique Lefebvre » 08 Oct 2008, 21:58
par Dominique Lefebvre » 08 Oct 2008, 21:58
Euler911 a écrit:Me*** je me suis fait encore avoir :hum:
Au fait sur wiki je li ça:

Il signifient quoi le K_b et les "crochets" du 2nd membre?
Le Kb est la constante de Boltzmann et les crochets signifient "valeur moyenne"

)
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 21:58
par Euler911 » 08 Oct 2008, 21:58
Dominique Lefebvre a écrit:Elle est proportionnelle à l'énergie cinétique moyenne d'une population d'atomes...
Donc il en faut au minimum 2? C'est un peu bizarre tout de même!
-
Skrilax
- Membre Relatif
- Messages: 426
- Enregistré le: 14 Juin 2008, 13:49
-
 par Skrilax » 08 Oct 2008, 21:58
par Skrilax » 08 Oct 2008, 21:58
Ah oui en effet je viens de me rendre sur la page wikipédia et c'est marqué..
-
Benjamin
- Membre Complexe
- Messages: 2337
- Enregistré le: 14 Avr 2008, 10:00
-
 par Benjamin » 08 Oct 2008, 21:59
par Benjamin » 08 Oct 2008, 21:59
Parlant de limite, je vous propose d'élargir quelque peu le sujet, et de parler de la limite du modèle des gaz parfait. PV=nRT est-il valable tout le temps et pourquoi ?
-
Babe
- Membre Irrationnel
- Messages: 1186
- Enregistré le: 06 Mai 2006, 10:52
-
 par Babe » 08 Oct 2008, 21:59
par Babe » 08 Oct 2008, 21:59
Euler911 a écrit:Me*** je me suis fait encore avoir :hum:
Au fait sur wiki je li ça:
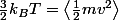
Il signifient quoi le K_b et les "crochets" du 2nd membre?
les crochets signifie "valeur moyenne"
en gros, étant donné que tu ne peux connaitre l' énergie de chaque particule (il y en a trop) il faut faire des moyennes
c'est ce qu'on appelle la physique statistique
 par Dominique Lefebvre » 08 Oct 2008, 22:01
par Dominique Lefebvre » 08 Oct 2008, 22:01
Euler911 a écrit:Donc il en faut au minimum 2? C'est un peu bizarre tout de même!
Non pas 2 !!tu fais des stats sur une population de 2 individus ? Disons plusieurs millions ! ce qui fait quand même une quantité de matière très petite (calcule le nombre de moles de gaz que cela représente!)
 par Dominique Lefebvre » 08 Oct 2008, 22:02
par Dominique Lefebvre » 08 Oct 2008, 22:02
Benjamin631 a écrit:Parlant de limite, je vous propose d'élargir quelque peu le sujet, et de parler de la limite du modèle des gaz parfait. PV=nRT est-il valable tout le temps et pourquoi ?
Ah oui, bonne idée. je les laisse réfléchir un peu...
 par Dominique Lefebvre » 08 Oct 2008, 22:03
par Dominique Lefebvre » 08 Oct 2008, 22:03
Je constate quand même que vos prof de physique ne vous racontent pas grand chose... C'est bien dommage!
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 22:04
par Euler911 » 08 Oct 2008, 22:04
Dominique Lefebvre a écrit:Non pas 2 !!tu fais des stats sur une population de 2 individus ? Disons plusieurs millions ! ce qui fait quand même une quantité de matière très petite (calcule le nombre de moles de gaz que cela représente!)
No comment... :marteau: :marteau:
Une autre chose lue sur wiki:
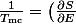_{V,N})
Je sais que les deltas bizarres sont des dérivées partielles mais les indices V et N veulent dire quoi(pourquoi sont-ils en indice)? C'est encore une histoire de valeur moyenne?
 par Dominique Lefebvre » 08 Oct 2008, 22:06
par Dominique Lefebvre » 08 Oct 2008, 22:06
Euler911 a écrit:No comment... :marteau: :marteau:
Une autre chose lue sur wiki:

Je sais que les deltas bizarres sont des dérivées partielles mais les indices V et N veulent dire quoi(pourquoi sont-ils en indice)? C'est encore une histoire de valeur moyenne?
Non, cela veut dire que l'on dérive la fonction en considérant que V (le volume) et N (le nombre de particules) sont des constantes pour la dérivation.
-
Babe
- Membre Irrationnel
- Messages: 1186
- Enregistré le: 06 Mai 2006, 10:52
-
 par Babe » 08 Oct 2008, 22:06
par Babe » 08 Oct 2008, 22:06
Benjamin631 a écrit:Parlant de limite, je vous propose d'élargir quelque peu le sujet, et de parler de la limite du modèle des gaz parfait. PV=nRT est-il valable tout le temps et pourquoi ?
ta question est elle:quelles approximations fais t-on dans le modèle du gaz parfait ?
-
Benjamin
- Membre Complexe
- Messages: 2337
- Enregistré le: 14 Avr 2008, 10:00
-
 par Benjamin » 08 Oct 2008, 22:06
par Benjamin » 08 Oct 2008, 22:06
Cela en fait parti oui, ce qui amène à la définition de la température légale.
 par Dominique Lefebvre » 08 Oct 2008, 22:09
par Dominique Lefebvre » 08 Oct 2008, 22:09
Babe a écrit:ta question est elle:quelles approximations fais t-on dans le modèle du gaz parfait ?
Je voyais cela plutôt comme : dans quelles conditions cette loi approximative n'est plus vraie?
Par exemple, de dilution....
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 22:10
par Euler911 » 08 Oct 2008, 22:10
Dominique Lefebvre a écrit:Je constate quand même que vos prof de physique ne vous racontent pas grand chose... C'est bien dommage!
Ben en fait, en Belgique, il n'y a pas beaucoup de prof de physique mais des profs de sciences... La plupart sont soit des biologistes ou des chimistes. Dans mon école, les profs de sciences enseignent les 3 matières (physique chimie et bio) même s'il n'ont "que" le diplôme dans une des matières.
Heureusement depuis l'année dernière j'ai la chance d'avoir une "vraie" physicienne (qui ne donne que physique) en cours... Et je dois dire que j'ai du mal! Ma moyenne est de 15/20 et je suis 2e de la classe (avant j'avait 18 env., sans vouloir être prétentieux), c'est dire si c'est devenu compliqué.
Bref,... ça doit être dur pour des biologistes de parler de toutes les finesses de la physique!
EDIT: j'ai oublié de dire que ma prof de physique est la seule de toute l'école à l'être parmi une dizaine de prof de sciences.
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 22:11
par Euler911 » 08 Oct 2008, 22:11
Dominique Lefebvre a écrit:Non, cela veut dire que l'on dérive la fonction en considérant que V (le volume) et N (le nombre de particules) sont des constantes pour la dérivation.
Ok, ok:D Merci!
J'en apprends des choses aujourd'hui:ptdr:
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 22:16
par Euler911 » 08 Oct 2008, 22:16
Dominique Lefebvre a écrit:Par exemple, de dilution....
A cause du volume?
-
Benjamin
- Membre Complexe
- Messages: 2337
- Enregistré le: 14 Avr 2008, 10:00
-
 par Benjamin » 08 Oct 2008, 22:29
par Benjamin » 08 Oct 2008, 22:29
Si tu n'as pas assez de particules, on retombe sur un problème de définition de température de toute façon. PV=nRT reste une loi macroscopique. Je pensais plutôt au problème inverse, que se passe-t-il si la pression augmente ?
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 22:40
par Euler911 » 08 Oct 2008, 22:40
Le question est adressée à qui?
-
Benjamin
- Membre Complexe
- Messages: 2337
- Enregistré le: 14 Avr 2008, 10:00
-
 par Benjamin » 08 Oct 2008, 22:55
par Benjamin » 08 Oct 2008, 22:55
A qui veut bien y répondre lol.
-
Euler911
- Membre Irrationnel
- Messages: 1486
- Enregistré le: 15 Aoû 2008, 17:14
-
 par Euler911 » 08 Oct 2008, 23:01
par Euler911 » 08 Oct 2008, 23:01
Mdr! J'y réfléchirais [si j'ai le temps] demain;)
Mais maintenant, il se fait tard!
Bonne fin de soirée à tous
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 18 invités