Bonjour!
J'ai une question de cours de thermodynamique toute simple sur laquelle je bloque pourtant depuis longtemps:
Sous quelle forme mathématique applique-t-on le premier principe?
Avec quelles hypothèses?
Delta U peut-il être calculé pour toute transformation?
Je pense que la réponse à la première question est : Delta U= W+ T
Hypothèses: système fermé, état initial et final en equilibre thermodynamique interne.
Par contre, la dernière question me pose problème... je suis tentée de répondre oui, mais la forme de la question implique que c'est plutôt non...
merci beaucoup de votre aide!
Lyse
Thermodynamique: premier principe
3 messages
- Page 1 sur 1
Bonsoir,
Pour la première question, il faudrait que tu précises à quoi correspondent les lettres. En général il me semble qu'on emploie pas le T mais plutôt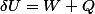 où Q est la quantité d'énergie mise en jeu sous forme de chaleur (transferts thermiques).
où Q est la quantité d'énergie mise en jeu sous forme de chaleur (transferts thermiques).
Pour la deuxième question, étant donné que la loi de la conservation de l'énergie est (jusqu'à maintenant) universelle, il me semble que l'on peut calculer la variation de l'énergie interne quelque soit la transformation.
Pour la première question, il faudrait que tu précises à quoi correspondent les lettres. En général il me semble qu'on emploie pas le T mais plutôt
Pour la deuxième question, étant donné que la loi de la conservation de l'énergie est (jusqu'à maintenant) universelle, il me semble que l'on peut calculer la variation de l'énergie interne quelque soit la transformation.
3 messages
- Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 17 invités
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
