Bonjour,
Je voudrais avoir quelques précisions à propos des solutions.
1.Qu'est-ce qu'une solution ?
2.Une solution est-elle forcément ionique ? Si oui, pourquoi ?
3.Qu'est-ce qu'une solution acqueuse ? C'est un solution qui contient des ions d'eau ?
Aussi, lorsque que deux solutions sont mélangées et qu'on y verse de l'eau, si un précipité est formé dans la solution acqueuse obtenue alors les ions de signes contraires des deux solutions ne peuvent pas coexister en solution.
Comment savoir lesquels des ions de chaque solution ne peut pas coéxister ?
Questions sur les solutions
4 messages
- Page 1 sur 1
Une solution est une dispersion d'un constituant ajouté (dit soluté) à un liquide dit solvant, de manière à ce que chaque molécule ou ion de ce soluté soit séparé de ses voisines par des molécules de solvant.
Une solution faite dans l'eau comme solvant est appelée aussi solution aqueuse.
Toute solution n'est pas forcément ionique. Le sel donne une solution ionique dans l'eau. Le sucre ne donne pas une solution ionique dans l'eau.
Seuls les acides, bases et sels donnent des solutions ioniques quand on les dissout dans l'eau. Ex.: NaCl, H2SO4, Ca(OH)2.
Les substances qui ne sont ni acides, ni bases, ni sels, se dissolvent dans l'eau sans former de ions. Ex.: H2O2, sucre, amidon.
L'eau ne forme pas de ions.
Quand tu mélanges deux solutions contenant des ions, tu procèdes par élimination pour savoir la formule du précipité. Tu pars de l'idée que certains ions ne font jamais de précipité. Ce sont : Na+, K+, NH4+, NO3^-. le préciupité est formé par les autres ions.
Une solution faite dans l'eau comme solvant est appelée aussi solution aqueuse.
Toute solution n'est pas forcément ionique. Le sel donne une solution ionique dans l'eau. Le sucre ne donne pas une solution ionique dans l'eau.
Seuls les acides, bases et sels donnent des solutions ioniques quand on les dissout dans l'eau. Ex.: NaCl, H2SO4, Ca(OH)2.
Les substances qui ne sont ni acides, ni bases, ni sels, se dissolvent dans l'eau sans former de ions. Ex.: H2O2, sucre, amidon.
L'eau ne forme pas de ions.
Quand tu mélanges deux solutions contenant des ions, tu procèdes par élimination pour savoir la formule du précipité. Tu pars de l'idée que certains ions ne font jamais de précipité. Ce sont : Na+, K+, NH4+, NO3^-. le préciupité est formé par les autres ions.
Non il peut effectivement être sous forme gazeuse (exemple: 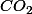 dissous) ou solide (ex: poudre de charbon actif).
dissous) ou solide (ex: poudre de charbon actif).
Attention cependant l'eau peut former des ions. Il y a une constante d'auto-ionisation de l'eau qui dépend de la température. A 25°C: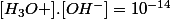 . Donc dans de l'eau pure, il y a
. Donc dans de l'eau pure, il y a 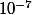 mol/L de
mol/L de 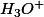 et
et 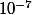 mol/L de
mol/L de 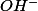 . Il y a toujours autant de charges + que de charges - en solution.
. Il y a toujours autant de charges + que de charges - en solution.
Pour déterminer par calcul à partir de quelle concentration certains ions s'assemblent pour former un précipité il faut utiliser les valeurs des constantes des produits de solubilité.
Attention cependant l'eau peut former des ions. Il y a une constante d'auto-ionisation de l'eau qui dépend de la température. A 25°C:
Pour déterminer par calcul à partir de quelle concentration certains ions s'assemblent pour former un précipité il faut utiliser les valeurs des constantes des produits de solubilité.
4 messages
- Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 1 invité
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
