Bonjour,
La chimie n'étant pas du tout mon domaine mais devant me poser certaines questions par rapport à ce produit, je me permets ce post sur le forum.
Je reçois actuellement des sacs de 25 kg de nitrate de sodium "dit" trés pur. La seule indication dont je dispose est une indication sur la fiche produit : "titre 99-100.5".
1ére question :
Je souhaiterais connaître la proportion de Na "pur" pour 1 kg de Na No3 ?
2éme question :
Ensuite ces 25 kg de nitrate de sodium sont mélangés dans 30 litres d'eau.
Je souhaiterais connaître alors la concentration en g/l de Na dans la solution (ça découle de la 1ére question directement, je devrais y arriver tout seul IoI) ?
Dernier point, je souhaiterais connaître la concentration de Na en nbr de mol/l ?
J'espère ne pas avoir dis trop de bétise et avoir donné suffisamment d'informations pour répondre aux questions.
Merci encore pour le temps que vous accorderez à ce post. Si vous pouviez accompagner vos réponses de quelques explications, je ferais progresser mon QI IoI
Merci d'avance.
Renaud.
Novice chimie : Quantité de Na dans le nitrate de Sodium Na No3
3 messages
- Page 1 sur 1
Salut
1ère question :
La proportion (en masse) est égale à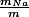
1 mole de NaNO3 donne 1 mole de Na et 1 mole de NO3 donc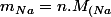}) et
et }})
Le proportion est donc le rapport des masses molaires.
Pour la 2ème question, on connaît la proportion de Na dans le NaNO3, la masse m de NaNO3 et le volume d'eau donc :
}}{M_{(NaNO_3)}} \; . \frac m V)
Et pour passer des grammes aux moles, on divise par la masse molaire.
1ère question :
La proportion (en masse) est égale à
1 mole de NaNO3 donne 1 mole de Na et 1 mole de NO3 donc
Le proportion est donc le rapport des masses molaires.
Pour la 2ème question, on connaît la proportion de Na dans le NaNO3, la masse m de NaNO3 et le volume d'eau donc :
Et pour passer des grammes aux moles, on divise par la masse molaire.
NaNO3
Na = 23.
NO3 = 14 + 48 = 62.
NaNO3 = 23 + 62 = 85.
Le rapport Na/NaNO3 = 23/85.
Dans 1 kg de NaNO3, il y a (23/85)1000 g de Na.
La suite ne peut pas être résolue. Si tu dissous 25 kg de NaNO3 dans 30 litres d'eau, tu ne peux pas connaître le volume de la solution que tu vas obtenir. Tu obtiendras plus de 30 litres de solution, mais moins de 55 litres. Et personne n'est en mesure de dire le volume de ta solution. Personne. Les volumes ne sont pas additifs en chimie. Les masses sont additives, certes, mais pas les volumes. Tu obtiendras bien 55 kg de solution. Mais on ne peut pas calculer le volume. Il faut le mesurer.
Donc on ne peut pas connaître la concentration que ce soit en grammes par litre, ou en mole par litre.
Désolé.
NO3 = 14 + 48 = 62.
NaNO3 = 23 + 62 = 85.
Le rapport Na/NaNO3 = 23/85.
Dans 1 kg de NaNO3, il y a (23/85)1000 g de Na.
La suite ne peut pas être résolue. Si tu dissous 25 kg de NaNO3 dans 30 litres d'eau, tu ne peux pas connaître le volume de la solution que tu vas obtenir. Tu obtiendras plus de 30 litres de solution, mais moins de 55 litres. Et personne n'est en mesure de dire le volume de ta solution. Personne. Les volumes ne sont pas additifs en chimie. Les masses sont additives, certes, mais pas les volumes. Tu obtiendras bien 55 kg de solution. Mais on ne peut pas calculer le volume. Il faut le mesurer.
Donc on ne peut pas connaître la concentration que ce soit en grammes par litre, ou en mole par litre.
Désolé.
3 messages
- Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 6 invités
Tu pars déja ?
Fais toi aider gratuitement sur Maths-forum !
Créé un compte en 1 minute et pose ta question dans le forum ;-)
Identification
Pas encore inscrit ?
Ou identifiez-vous :
