Avancement maximal, final, taux d'avancement final
Peut-on mélanger l'huile et l'eau ? Posez vos questions de chimie ici
-
Anonyme
 par Anonyme » 24 Nov 2007, 21:26
par Anonyme » 24 Nov 2007, 21:26
Bonsoir, j'ai besoin d'aide...
Voici l'énoncé: Une solution aqueuse (s1) d'acide ascorbique C6H8O6 de concentration en solution aqueuse c1=1.0.x10^-3 mol.L a un pH de 3,6. Une solution (s2) d'acide ascorbique de concentration en soluté apporté c2=1.0x10^-4 mol.L a un pH de 4,2.
a-Ecrire l'équation de la réaction de l'acide ascorbique avec l'eau.
C6H8O6+H2O=C6H7O6(-)+H3O(+)
b-La transformation est-elle totale ? Justifier.
c-Déterminer pour chacune des deux solutions le taux d'avancement final de la reaction de l'acide avec l'eau.
d-Comparer les résultats et conclure quant à l'effet de la dilution sur le taux d'avancement final de la reaction de l'acide avec l'eau.
Voilà je n'arrive pas a faire la b, car ca me gene ya pas le volume pour calculer xmax.
Merci
-
Furi0u5
- Membre Relatif
- Messages: 449
- Enregistré le: 15 Oct 2005, 16:44
-
 par Furi0u5 » 24 Nov 2007, 22:49
par Furi0u5 » 24 Nov 2007, 22:49
Salut
Montre que xéq = xmax, car il faut que 1.0.x10^-3 mol.L - xmax=0
-
Furi0u5
- Membre Relatif
- Messages: 449
- Enregistré le: 15 Oct 2005, 16:44
-
 par Furi0u5 » 25 Nov 2007, 01:39
par Furi0u5 » 25 Nov 2007, 01:39
Salut
pH = -log[C6H8O6] = 3.6
Donc 10^-3.6 =2.51x10^-4
ALors le taux d'avancement est: T = 2.51x10^-4 / 1.0x10^-3
T < 1
Donc la transformation n'est pas totale.
Ca devrait etre ça lol :we:
Bonne nuit :dodo:
-
Mari0n
- Membre Naturel
- Messages: 60
- Enregistré le: 10 Jan 2007, 18:43
-
 par Mari0n » 25 Nov 2007, 12:24
par Mari0n » 25 Nov 2007, 12:24
Pourquoi on divise par 1.0x10^-3 ? puisque c'est xf/xmax
-
Anonyme
 par Anonyme » 25 Nov 2007, 12:33
par Anonyme » 25 Nov 2007, 12:33
Pourquoi on divise par 1.0x10^-3(la concentration), alors que T=xf/xmax

-
raito123
- Habitué(e)
- Messages: 2102
- Enregistré le: 04 Nov 2007, 02:29
-
 par raito123 » 25 Nov 2007, 13:03
par raito123 » 25 Nov 2007, 13:03
Donc tu cherches si la transformation est compléte pour les deux solutions.
Les multiples ne doivent pas être utilisés sans nécessité

-
raito123
- Habitué(e)
- Messages: 2102
- Enregistré le: 04 Nov 2007, 02:29
-
 par raito123 » 25 Nov 2007, 13:23
par raito123 » 25 Nov 2007, 13:23
Voilà je n'arrive pas a faire la b, car ca me gene ya pas le volume pour calculer xmax.
Tu n'as pas besoin du volume puisque tout les reactifs sont dans le même volume. tu n'as alors que diviser par
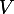
le volume pour travailler avec
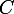
la concentration
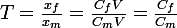
Les multiples ne doivent pas être utilisés sans nécessité
-
Anonyme
 par Anonyme » 25 Nov 2007, 13:38
par Anonyme » 25 Nov 2007, 13:38
Oui en effet je viens de comprendre, je suis à la question d.
Comparer les résultats et conclure quant à l'effet de la dilution sur le taux d'avancement final de la reaction de l'acide avec l'eau.
J'ai trouver pour s1=25% et s2=63%

-
raito123
- Habitué(e)
- Messages: 2102
- Enregistré le: 04 Nov 2007, 02:29
-
 par raito123 » 25 Nov 2007, 14:16
par raito123 » 25 Nov 2007, 14:16
Ouis c'est ça.
Les multiples ne doivent pas être utilisés sans nécessité
-
Anonyme
 par Anonyme » 25 Nov 2007, 15:05
par Anonyme » 25 Nov 2007, 15:05
Qu'est ce qu'on peut dire de la question d ?

-
raito123
- Habitué(e)
- Messages: 2102
- Enregistré le: 04 Nov 2007, 02:29
-
 par raito123 » 25 Nov 2007, 16:06
par raito123 » 25 Nov 2007, 16:06
plus la concentration de l'acide est forte plus ...
termines!
Les multiples ne doivent pas être utilisés sans nécessité
-
Anonyme
 par Anonyme » 25 Nov 2007, 16:47
par Anonyme » 25 Nov 2007, 16:47
J'ai mis plus la solution est diluée, plus on se rapproche d'une transformation totale, vue que le taux d'avancement pour s2 se rapproche de 1
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 1 invité
